АНТИБАКТЕРИАЛЬНОЕ ДЕЙСТВИЕ КФС №1 «АНТИПАРАЗИТАРНЫЙ» И №2 «ДЕТОКС» С 8-Ю ЭЛЕМЕНТАМИ
Плехова Наталья Геннадьевна, д.б.н., профессор ФГБОУ ВО
«Тихоокеанский государственный медицинский университет» Минздрав России
Радькова Людмила Ивановна, врач-терапевт, физиотерапевт, психолог,
педагог, спикер Компании, г. Владивосток
КФС Корректоры функционального состояния (КФС Кольцова) предназначены для генерирования внешнего электромагнитного поля и созданы на основе киральных элементов с промежуточными слоями диэлектрика. Это низкоинтенсивные генераторы продольных волн, которые способны целенаправленно изменять функциональное состояние биообъекта малыми, постоянно действующими воздействиями.
Корректоры не экранируют внешнее электромагнитное излучение, а изменяют его в пространственно-временную структуру, совместимую со структурной организацией био системы.
КФС Кольцова адаптивно реагируют, в первую очередь, на изменение всех внешних ориентационных связей, порождаемых спиновыми, гравитационными, электромагнитными взаимодействиями. Экспериментально доказано, что КФС обладают свойством бесконтактной активации жидких сред. Создание корректоров защищено патентами РФ, как устройство для коррекции функцинального состояния биообъекта [1], как устройство для активации жидких сред [2], как устройство для коррекции внешнего электромагнитного поля, воздействующего на живой организм [3]. В КФС, изготовленном по принципу скалярного магнитного поля, кванты электромагнитного поля, попав в его пара или ферромагнетик, наводят в нем магнитное поле. При этом электроны ориентируются по силовым линиям магнитного поля и усиливают внешние поля в парамагнетике или ферромагнетике.
При создании КФС №1 «АНТИПАРАЗИТАРНЫЙ» нового поколения с 8-ю элементами, учитывалось свойство биосистем резонансно откликаться на биологически значимые многочастотные воздействия информационного характера. В нем прописаны образы лекарственных растений и минералов, которые богаты сбалансированными комплексами природных биологически активных веществ и обладают целебными свойствами.
В КФС №2 «ДЕТОКС» прописана поляризация образов композиции из 20-ти трав, таких как флавит, живица хвойных деревьев, а также растений для поднятия иммунитета и восстановления обмена веществ амаранта (листья, соцветия, масло), нони, кудина, крапивы, морских водорослей, топинамбура, илецкой соли, сибирского бальзама на меде диких пчел с добавлением сибирских трав от опухолей и заболеваний щитовидной железы. Прописан канал Космической Теургии «МАЙЯ» БУЛ, предназначенный для выведения токсических веществ из организма.
Наиболее доступные модели для понимания механизма сверхслабого воздействия являются такие объекты как прокариоты (бактерии). В нашем исследовании мы сочли возможным изучить воздействие КФС на стафилококки, по причине высокой заболеваемости населения Земли. Золотистый стафилококк (лат. Staphylococcus aureus) — вид шаровидных грамположительных бактерий из рода стафилококков. Приблизительно 25—40 % населения являются постоянными носителями этой бактерии, которая может сохраняться на кожных покровах и слизистых оболочках верхних дыхательных путей [4].
Стафилококки – род шаровидных неподвижных аспорогенных грамположительных хемоорганотрофных факультативно-анаэробных или аэробных бактерий из семейства Micrococcaceae. В роду Staphylococcus выделяют около 30-ти видов, при этом 14 обнаружены на коже и слизистой человека, включая S. aureus, S. epidermidis, S. saprophyticus. Для видовой идентификации используют, в основном, 3 теста: продукцию плазмокоагулазы, анаэробную ферментацию маннита и глюкозы. Антигенная структура бактерии сложная, видоспецифичными антигенами являются тейховые кислоты. S. aureus может вызывать широкий диапазон заболеваний, начиная с лёгких кожных инфекций: угри, импетиго (может быть вызван также и Streptococcus pyogenes), фурункул, флегмона, карбункул, стафилококковый ожогоподобный кожный синдром (англ.) и абсцесс — до смертельно опасных заболеваний: пневмония, менингит, остеомиелит, эндокардит, инфекционно-токсический шок и сепсис.
Диапазон заболеваний простирается от кожных, мягких тканей, респираторных, костных, суставных и эндоваскулярных до раневых инфекций. Он до сих пор является одной из четырёх наиболее частых причин внутрибольничных инфекций, часто вызывая послеоперационные раневые инфекции. В последние годы определенный интерес представляет исследование взаимоотношений между этими бактериями и факторами неспецифической защиты слизистых оболочек, к которым относятся клетки врожденного иммунитета.
Материалы и методы
S. aureus метициллинрезистентный (MRSA, ГКПМ-Оболенск) инкубировали на кровяном агаре в термостате при 37 °С в течение 24ч, затем по стандарту мутности готовили концентрацию бактерий до 1 млн/мл карбонатно-бикарбонатным буфером (рН 9,5). Культуру St. aureus окрашивали акридиновым оранжевым (25 нг/мл) в течение 30-ти мин. и осаждали путем центрифугирования в течение 25 мин. при 1000 об/мин., после этого дважды отмывали в 10 мл фосфатно-солевого буфера (ФСБ, рН 7,4). Концентрацию бактерий доводили до 500 млн/мл по стандарту мутности и добавляли к клеткам в соотношении 1:20. Клетки вместе с бактериями без и привоздействии КФС инкубировали при 37 0С в течение 30 мин., для удаления непоглощенных фагоцитами микроорганизмов дважды отмывали путем центрифугирования в течение 10 мин. при 1000 об/мин., после чего продолжали инкубировать в течение 2-х и 4-х часов.
Для определения бактерицидного воздействия КФС аликвоты по 10 мкл в трех повторах неразбавленной суспензии и семи ее разведений (от 101 до 107) разносили в чашки Петри с кровяным агаром, инкубировали в течение 18 ч при 37 °С и визуально подсчитывали количество колоний. Выполнено три параллельных эксперимента.
Статистический анализ результатов проводили с помощью Statistica 8.0 (StatSoft, США). Все значения представлены как среднее арифметическое ± стандартная ошибка среднего (M±m). Данные по группам проанализированы с помощью t-критерия Стьюдента и Ньюмана-Кейлса для множественных сравнений со степенью доверительной вероятности 95% и выше (p<0.05).
Результаты исследования
Оценка бактерицидной активности КФС проводилась на модели «in vitro» с использованием воздействия в течение 15, 30 и 45 мин. Количественный учет КОЕ бактерий через 24 ч инкубации показал бактерицидную активность
КФС №2 ДЕТОКС и КФС «ФУНГИМИН» (3 на диаграммах).
Коагулозоположитепльные стафилококки это грамположительные каталазоположительные микроорганизмы, которые образуют типичные колонии на селективно-диагностической питательной среде, дающие положительную реакцию на коагулазу (S. аureus; S. aureus spp. anaerobius) или специфическую для кроличьей плазмы реакцию на агаре с кроличьей плазмой и фибриногеном при определении стандартным методом (Рис. 1).
Рис. 1. Колония Staphylococcus aureus на кровяном агаре

Staphylococcus aureus образует ацетоин и ферментирующие мальтозу в аэробных условиях в процессе определения этих биохимических тестов стандартным методом. Бактериальные клетки диаметром 0,5-1,5 мкм делятся в нескольких плоскостях несимметрично, образуя скопления, напоминающие гроздья винограда. Встречаются одиночные клетки, пары и тетрады. Клеточная стенка содержит пептидогликан и глицеринтейховую кислоту. Стафилококки формируют гладкие колонии, окрашенные каротиноидами в желтый или оранжевый цвета. Однако пигментирование не является видовым признаком.
При росте на желточно-солевом агаре образуются мутные круглые ровные колонии кремового, желтого или оранжевого цвета (Рис. 2).
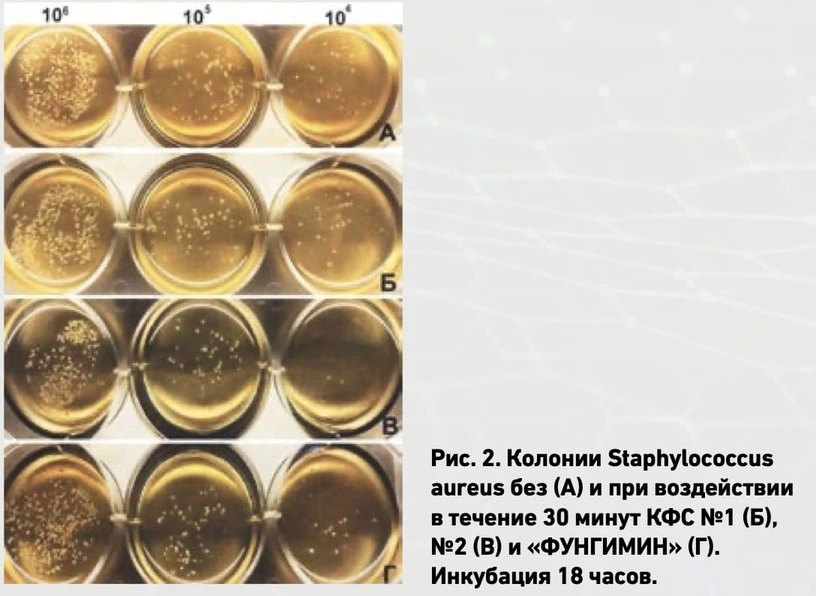
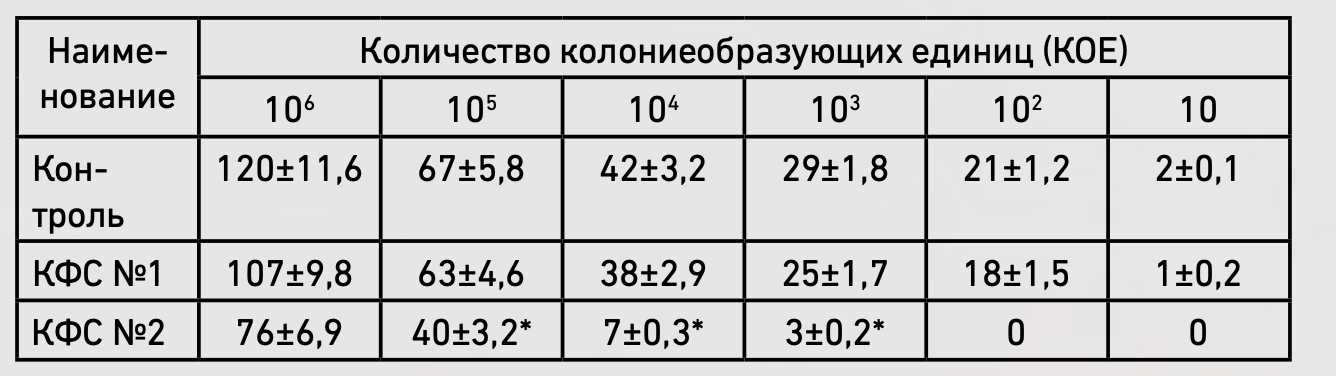
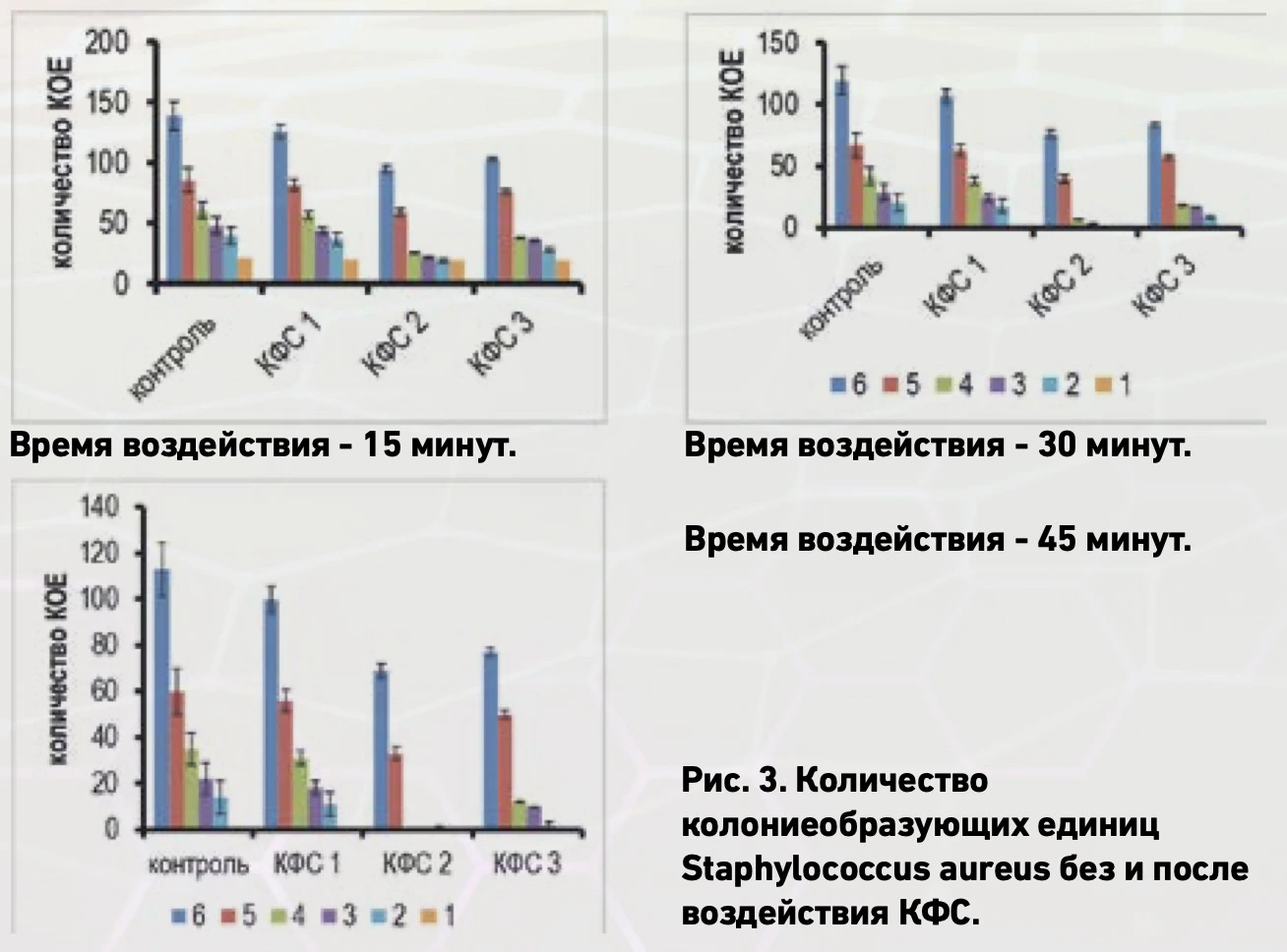
На Рис. 3 представлено число колоний после контакта с КФС, полученных при различном времени воздействия. Достоверное уменьшение числа колоний было обнаружено после воздействия КФС №2 и КФС «ФУНГИМИН», наиболее выраженное после 30 и 45 мин при всех разведениях. Как показано в таблице 1, после воздействия КФС №2 в течение 30 мин определялось минимальное количество колоний. Так, при разведении в тысячу раз изначальной концентрации 109 КОЕ/мл число составило 76±6,9, тогда как без воздействия 120±11,6.
Практически все бактерии погибали при больших разведениях после воздействия КФС 2, тогда как после воздействия КФС №1 отмечено увеличение числа КОЕ в 1,5 раз (Рис. 2, 3). Подобные результаты были получены при условии совместного культивирования образцов с суспензией бактерий в 1% в 10 мМ фосфатно-солевом буфере с 10% сывороткой крови.
Таблица 1. Количество колониеобразующих единиц Staphylococcus aureus после 30 минутного воздействия
Название бактерия получила благодаря своему внешнему виду под микроскопом: в отличие от большинства бактерий, которые бесцветны, Staphylococcus aureus имеет золотистый цвет, обусловленный пигментами из группы каротиноидов. Интерес представляют исследования при воздействии КФС на бактерии, которые были поглощены клетками врожденного иммунитета.
Фагоцитоз определяли в отношении Staphylococcus aureus, предварительно окрашенных акридиновым оранжевым. Известно, что этот краситель способен проникать через поврежденную мембрану, маркируя гибнущие клетки флуоресценцией в желто-красном диапазоне. На Рис. 4 представлены клетки с фагоцитированными бактериями. Также был определен рост бактерий после совместной 4-х инкубации с клетками врожденного иммунитета.
Заключение. Многочисленные исследования сверхслабых воздействий на живые системы показывают, что для выявления механизма их воздействия необходимо привлекать качественно иные представления. Эти представления отличаются от понимания прямого внешнего воздействия на отдельные биологически важные системы организма [5]. Биологическую значимость сверхслабых воздействий можно рассматривать на примерах их влияния на протекание биохимических и физиологических процессов, что определяет вполне оправданный феноменологический подход.
Понимание того, являются ли сверхслабые воздействия обычной статистической единицей или практически информационной матрицей протекания биохимических процессов, является исходным положением при выяснении биологической сущности.

















































